
Van lego tot bewustzijn: Hoe jouw brein pijn aanmaakt
Stel je voor: je stoot je teen tegen de tafelpoot. Of je stapt in het donker op dat legosteentje. Je weet wel. Dat ene.
Binnen een fractie van een seconde voel je pijn. Maar wat gebeurt er eigenlijk precies tussen dat moment van stappen en dat moment van ‘oh shit'?
Het antwoord is fascinerend, en vertelt ons waarom pijn soms zo hardnekkig kan zijn, zelfs als het weefsel al lang genezen is. Omdat pijn geen directe afspiegeling is van weefselschade, maar het resultaat van verwerking. Je brein maakt pijn.
In deze tekst neem ik je mee op reis door dat systeem. Je gaat in deze tekst een boel namen en routes lezen. Zie het als een reisgids: per traject krijg je de wetenswaardigheden en bezienswaardigheden. Je hoeft niet alles te onthouden, zolang je maar snapt hoe het landschap eruitziet.
Lonely Planet? Nee. Lonely Pain.
De Roadtrip:
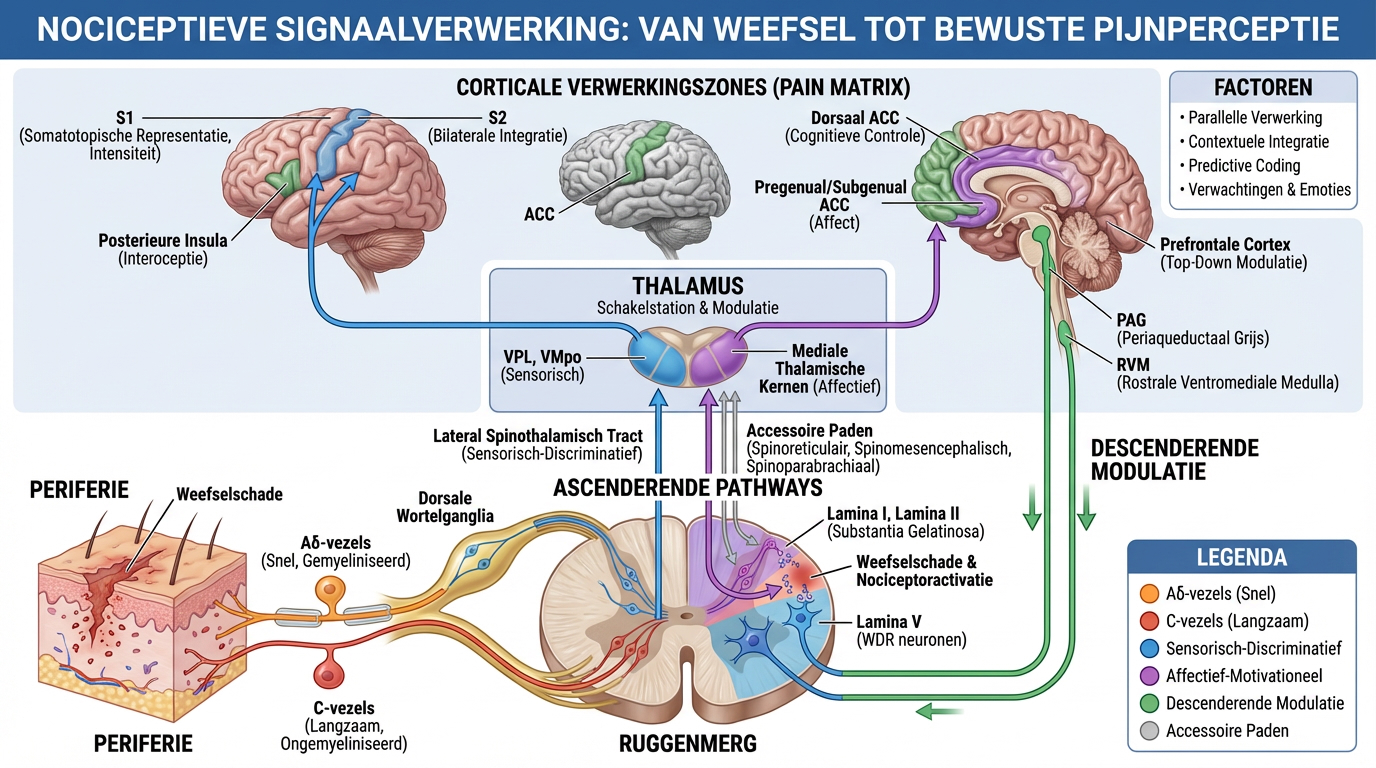
Het begint met de alarminstallatie (en nog geen pijn)
In huid, spieren en gewrichten bevinden zich miljoenen gespecialiseerde sensorische cellen: nociceptoren. Ze worden vaak pijnreceptoren genoemd, maar strikt genomen zijn ze dat niet. Nociceptoren registreren geen pijn, maar fysische en chemische omstandigheden die samenhangen met (dreigende) weefselschade, zoals extreme hitte of kou, hoge mechanische belasting, verzuring en ontstekingsmediatoren. Het zijn de sensoren in je lijf die de signalen doorgeven ‘er is hier iets, ik weet niet wat, maar er is hier iets’.
Ze registreren geen pijn, ze registreren mogelijk gevaar.
Wanneer nociceptoren worden geactiveerd, genereren zij elektrochemische signalen die via perifere zenuwvezels naar het centrale zenuwstelsel worden geleid. Deze signalen coderen stimulus eigenschappen — niet pijn als bewuste ervaring. Of deze input uiteindelijk tot pijn leidt, wordt pas later in het verwerkingsproces bepaald en is afhankelijk van centrale verwerking en modulatie (Basbaum et al., 2009). Met andere woorden: het alarm wordt getriggerd, maar of er hard of zacht of niet wordt geloeid, dat beslist het brein.
Nociceptieve informatie bereikt het centrale zenuwstelsel hoofdzakelijk via twee typen vezels. Aδ-vezels zijn dun gemyeliniseerd en geleiden relatief snel. Zij dragen bij aan de scherpe, goed te lokaliseren eerste pijn. Het legoblokje-awareness moment. C-vezels zijn ongemyeliniseerd en geleiden traag. Zij zijn betrokken bij de doffe, brandende tweede pijn die later ontstaat en langer aanhoudt. Het hinkelen-op-een-been-oooooooooohhh-neeee moment (Peirs & Seal, 2016).
Belangrijk is dat geen van deze vezels zelf pijn veroorzaakt. Ze leveren informatie. Pijn ontstaat pas wanneer het centrale zenuwstelsel die informatie interpreteert als reden voor bescherming.
Eerste checkpoint: het ruggenmerg
De nociceptieve signalen worden vanuit de periferie geleid via de cellichamen in het dorsale wortelganglion — een anatomisch tussenstation net buiten het ruggenmerg — en komen vervolgens binnen in de dorsale hoorn van het ruggenmerg. Hier vindt al substantiële, actieve verwerking plaats; dit is geen passieve doorgeefroute.
👓 Bekijk het ruggenmerg in de figuur: je ziet hoe de Aδ- en C-vezels (oranje en rood) vanuit de periferie via de dorsale wortelganglion het ruggenmerg binnenkomen.
In de dorsale hoorn eindigen Aδ- en C-vezels voornamelijk in lamina I en II, de meest oppervlakkige lagen, gezamenlijk aangeduid als de substantia gelatinosa vanwege hun karakteristieke histologische gelei achtige structuur (Kuner & Flor, 2016). In deze lagen bevinden zich gespecialiseerde neuronen die selectief reageren op noxische prikkels, zoals extreme hitte, hoge mechanische belasting of langdurige stimulatie.
Dieper in de dorsale hoorn, met name in lamina V, bevinden zich de zogenoemde wide dynamic range (WDR)-neuronen. Deze neuronen zijn een beetje de oplichters van het traject, ze reageren op álles: van lichte tactiele stimulatie tot uitgesproken nociceptieve signalen. Zij fungeren als integratie-knooppunten, waarin verschillende afferente signalen worden samengebracht en functioneel gewogen.
Bij herhaalde nociceptieve input of bij inflammatie verschuift hun drempel en versterkt hun respons op tactiele prikkels - een mechanisme dat bijdraagt aan mechanische allodynie. Dan voelt je merino wollen shirt alsof het van schuurpaier gemaakt is.
Binnen de spinale lagen vindt al cruciale modulatie van nociceptieve signalen plaats. Interneuronen spelen hierbij een centrale rol: zij kunnen signalen remmen, maar in sommige circuits ook versterken, afhankelijk van de specifieke verbindingen en prikkelcontext.
Lokale modulatie gebeurt bijvoorbeeld via Aβ-tactiele vezels. Tactiele input, zoals wrijven over de huid, activeert deze vezels en de bijbehorende interneuronen, waardoor de transmissie van nociceptieve signalen naar opstijgende banen wordt verminderd. Dit is waarom je automatisch over je voetzool wrijft nadat je op die lego bent gaan staan – niet omdat je moeder ooit zei dat het hielp, maar omdat je brein weet dat die extra tactiele input het nociceptieve signaal kan dempen. Op deze manier beïnvloedt lokale input al vroeg in het ruggenmerg wat uiteindelijk richting het brein wordt doorgegeven.
Daarnaast kunnen descenderende banen vanuit supraspinale structuren, zoals het PAG-RVM-systeem, de nociceptieve transmissie moduleren. Afhankelijk van context en neuronale toestand kan dit remmend of juist faciliterend zijn, waardoor de dorsale hoorn functioneert als een dynamisch regulatiecentrum waarin perifere signalen continu worden aangepast
👓 Let op in de figuur hoe de descenderende groene pijl van het PAG-RVM systeem precies op deze laminae aankomt
Dit is tevens het aangrijpingspunt van descenderende modulatie, onder andere via het PAG-RVM-systeem. Deze banen projecteren naar de dorsale hoorn en kunnen de activiteit van lamina I, II en V beïnvloeden. Afhankelijk van context en type neuronen kan deze modulatie inhiberend of faciliterend zijn.
Samen laten deze mechanismen zien dat de dorsale hoorn functioneert als een dynamisch regulatiecentrum, waar nociceptieve input wordt geïntegreerd en aangepast voordat deze verder opstijgt naar hogere centra. Deze filtering gebeurt zowel lokaal via interneuronen — bijvoorbeeld het klassieke gate control-principe, waarbij tactiele input nociceptieve signalen kan remmen — als supraspinaal via descenderende banen.
De gate control-theorie illustreert kernachtig hoe spinale circuits signalen selectief kunnen versterken of onderdrukken (Melzack & Wall, 1965, ze waren hun tijd ver vooruit). Moderne inzichten laten zien dat dit principe wordt uitgebreid door complexe interacties met descenderende modulatie en contextafhankelijke centrale processen.
De snelweg naar boven: niet één weg, maar een netwerk
Vanuit het ruggenmerg gaat het signaal omhoog via meerdere parallelle routes – en dat is cruciaal om te begrijpen. Er is geen enkele "pijnkabel" naar je hersenen. In plaats daarvan splitst de informatie zich in verschillende ascenderende pathways (=letterlijk stijgende paden). Elke baan heeft een specifieke bestemming en functie, waardoor signalen op meerdere niveaus tegelijk worden verwerkt en geïntegreerd. Het is alsof je het nieuws niet via één zender ontvangt, maar tegelijkertijd via Radio 1, het NOS TV journaal, en een Whatsapp channel.
👓 Kijk naar de figuur: je ziet hoe vanuit het ruggenmerg drie hoofdroutes (blauw, paars en grijs) naar verschillende delen van de thalamus projecteren.
Een belangrijk onderscheid bij de ascendenten pathways wordt gemaakt tussen laterale en mediaal/mediale banen:
•Laterale banen voeren informatie naar de somatosensorische cortex en zijn verantwoordelijk voor het nauwkeurig lokaliseren van pijn, evenals de intensiteit en kwaliteit van de stimulus. Deze route zorgt ervoor dat je precies kunt aangeven waar het pijn doet en hoe scherp of brandend het voelt. De ‘waar en hoeveel’ - route.
•Mediale banen projecteren naar limbaire structuren en andere associatieve gebieden in de hersenen. Deze routes spelen een rol bij de emotionele en affectieve aspecten van pijn, zoals onaangenaamheid, angst en alertheid. Mediale pathways koppelen sensorische input aan motivatie en gedragsreacties. De ‘oh shit dit is erg’ - route.
We bespreken drie routes van de ascending pathways.
Lateral spinothalamisch
Medial spinothalamisch
de aanvullende routes
1. De lateral spinothalamische route: "Waar doet het pijn, en hoeveel?"
Dit is de snelste en meest directe route. Neuronen uit lamina I kruisen naar de andere kant van het ruggenmerg en schieten via de anterolaterale columna omhoog naar de thalamus, het grote schakelstation diep in je hersenen.
👓 Volg in de figuur de blauwe lijn vanaf het ruggenmerg naar de thalamus.
Binnen de thalamus zijn er twee belangrijke bestemmingen: de VPL- en de VMpo kernen (Almeida et al., 2004):
1: VPL (ventro-posterior lateral): Deze kern projecteert naar de primaire somatosensorische cortex (S1) en de secundaire somatosensorische cortex (S2).
Dit systeem is geobsedeerd door details: waar precies zit die pijn? Hoe intens is het? Hoe lang duurt het? Scherp of dof? S1 heeft een prachtige somatotopische kaart – je linker grote teen heeft letterlijk zijn eigen plekje in je rechter hersenhelft. Dankzij dit systeem kun je met gesloten ogen precies aanwijzen waar die mug je gestoken heeft (Mancini et al., 2012).
2: VMpo (ventro-posterior medial, parvocellular): Dit is een relatief recent ontdekte kern – we snapten pas vanaf de vroege jaren 2000 hoe belangrijk deze is (Craig, 2009). Craig beschreef dit gespecialiseerd thalamisch gebied (VMpo) dat zou projecteren naar de posterieure insula voor interoceptieve aspecten van pijn. Dit model wordt nog steeds actief onderzocht en gedebatteerd, waarbij de meeste onderzoekers pijnverwerking beschouwen als een meer gedistribueerd netwerk van meerdere thalamocorticale routes.
👓 In de figuur zie je hoe VMpo een aparte route heeft naar de posterieure insula
Dat is een gebied dat gespecialiseerd is in interoceptie: het voelen van je lichaam van binnenuit. Niet "waar" en "hoeveel", maar "hóé voelt dit?" Die nare, moeilijk te beschrijven kwaliteit van pijn – dat misselijke, beklemmende gevoel dat bij hevige pijn hoort – dat komt grotendeels uit dit systeem (Craig, 2015). Het verschil tussen ‘mijn voet doet pijn’ en ‘ik voel me k.. ‘.
2. De mediale spinothalamische route: "Dit is belangrijk en ik vind het vreselijk"
Andere neuronen uit het ruggenmerg nemen een meer diffuse route naar mediale thalamische kernen (centrum medianum, parafasciculaire nucleus).
👓 Volg in de figuur de paarse lijn: deze projecteert naar een heel ander netwerk dan de blauwe sensorische route:
- Anterieure cingulate cortex (ACC): Het affectieve hart van pijnverwerking. De ACC zegt niet "au", maar "au!!!" – het geeft de emotionele lading, de drang om iets te dóen, de onplezierigheid van pijn. Imaging studies laten zien dat de ACC correleert met hoe erg mensen pijn vinden, meer dan met de fysieke intensiteit (Shackman et al., 2011).
- Prefrontale cortex: Hier komt betekenis bij. "Is dit gevaarlijk?" "Moet ik in paniek raken?" "Of is dit normaal postoperatief herstel?" De PFC moduleert hoe bedreigend je het signaal interpreteert (Lorenz et al., 2003). Het is je persoonlijke risico-analist.
- Amygdala: Het emotionele geheugen. Als pijn eerder gepaard ging met trauma, angst of hulpeloosheid, kleurt dat de huidige ervaring. De amagdyla vergeet nooit een goede ramp.
3. De accessoire routes: de AAA - arousal, autonomie en actie
Daarnaast zijn er de spinoreticulaire, spinomesencephalische en spinoparabrachiale pathways (Todd, 2010; Gauriau & Bernard, 2002).
Deze projecteren naar de hersenstam en het periaqueductale grijs (PAG) en zorgen voor:
Arousal - Verhoogde alertheid ("WAKKER WORDEN, er is iets mis!”)
Autonomie - Autonome reacties (hartslag omhoog, zweten, pupilverwijding)
Actie - Motorische voorbereidingen (terugtrekreflex, beschermend gedrag)
Dit zijn de systemen die je lichaam in staat van paraatheid brengen voordat je bewust beseft wat er aan de hand is. Je hand trekt zich terug van de hete pan voordat je hebt bedacht: "Oei, dat is heet."
Thalamus: dirigent van het bewustzijn
Zodra nociceptieve signalen de hersenen bereiken, komen ze eerst aan bij de thalamus, een centraal schakelstation. De thalamus ontvangt input van zowel laterale als mediale ascenderende banen en verdeelt deze vervolgens naar specifieke corticale en subcorticale gebieden. N soort verkeersagent, maar dan een die de wegen aanpast terwijl het verkeer rijdt.
De thalamus is geen passief doorgeefluik. De thalamus fungeert als informatie-integrator: het verwerkt, filtert en organiseert signalen zodat de cortex en andere hersengebieden relevante, coherente input ontvangen.
Het is een actief filter- en modulatiestation dat bepaalt wélke informatie doordringt tot bewust bewustzijn en wélke genegeerd wordt (Apkarian et al., 2005). Signalen worden hier versterkt of onderdrukt afhankelijk van context: ben je onder narcose? Diep in slaap? Geconcentreerd op een belangrijke taak? De thalamus houdt de wacht.
En die poort wordt niet alleen van onderaf (bottom-up) aangestuurd, maar ook van bovenaf (top-down). Je hersenschors stuurt continu signalen terug naar de thalamus: "Ja, dit is belangrijk, laat het door" of "Nee, dit kunnen we negeren." Dit is waarom je pijn kunt vergeten tijdens een voetbalwedstrijd en hem pas voelt als je erna onder de douche staat. Of waarom je die hoofdpijn plotseling voelt zodra de vergadering eindelijk afgelopen is.
De hersenschors: waar signaal pijn wordt
En dan komen we bij het meest fascinerende deel: de corticale verwerking. Want hier, in de hersenschors, gebeurt het eigenlijke wonder (of de vloek): het brein maakt een bewuste, subjectieve ervaring van pijn.
Dit gebeurt niet in één gebied, maar in een gedistribueerd netwerk van gebieden die parallel en interactief werken. Mensen noemen dit soms de "pain matrix", hoewel dat een misleidende term is – want ditzelfde netwerk wordt bij andere aandachttrekkende, bedreigende of emotioneel geladen prikkels ook getriggerd (Legrain et al., 2011).
Het is niet een pijn-specifiek systeem. Het is eerder een "salience network": een systeem dat zegt “Dit verdient aandacht.” (en wat er daarna voor reactie op komt, verschilt)
Binnen dit netwerk heeft elk gebied zijn rol:
- S1 leest de kaart: links grote teen, 7 op de 10, scherp, constant
- S2 vergelijkt met eerdere ervaringen en integreert bilateraal
- Posterieure insula voelt het als een lichamelijke sensatie, een verandering in hoe je lichaam is
- Anterieure insula evalueert: "Is dit erg? Moet ik me zorgen maken?"
- ACC voegt de emotie toe: onplezierig, vervelend, ónacceptabel, affreus
- Prefrontale cortex denkt na: "Wat betekent dit? Wat moet ik doen?"
Deze gebieden praten continu met elkaar. Ze construeren samen de ervaring die we "pijn" noemen – en die constructie is gevoelig voor context, verwachtingen, emoties en betekenis (Wiech, 2016). Pijn is geen passieve registratie, maar een actieve productie van je brein.
Het brein voorspelt, het brein moduleert
Moderne neurowetenschap denkt niet meer in termen van "informatie komt binnen → brein verwerkt → gevoel komt eruit.” Dat is zo jaren 80.
Moderne neurowetenschappelijke modellen suggereren dat het brein volgens principes van predictive coding werkt (Baliki & Apkarian, 2015). Volgens dit theoretisch framework genereert het brein constant voorspellingen over wat er gáát gebeuren in je lichaam. Wanneer signalen van onderaf binnenkomen, vergelijkt het brein die met de verwachting.
Mismatches tussen voorspelling en werkelijkheid – prediction errors – krijgen aandacht, vooral wanneer ze wijzen op iets dat relevant is voor lichaamsintegriteit. Of het brein zo'n mismatch interpreteert als pijn hangt af van hoe belangrijk of bedreigend die fout wordt ingeschat.
Dit verklaart waarom:
- Nocebo werkt : verwacht je pijn, dan voel je meer pijn
- Placebo werkt : verwacht je verlichting, dan dempt je brein de signalen
- Aandacht zo krachtig is : waar je op let, wordt versterkt; wat je negeert, verzwakt
- Betekenis zo cruciaal is : pijn die je begrijpt en kunt plaatsen is minder bedreigend
En het brein kan niet alleen de perceptie van pijn beïnvloeden, maar ook de transmissie ervan op lagere niveaus. Het heeft een afstandbediening voor het eigen alarmsysteem.
De rem: descenderende modulatie
Want terwijl al die signalen omhoog vliegen, is er ook een krachtig systeem dat van boven naar beneden werkt: de descenderende pijnmodulatie (Ossipov et al., 2010).
👓 In de figuur zie je dit als de groene pijlen die van de hersenstam (PAG en RVM) terug naar het ruggenmerg lopen.
Vanuit het periaqueductale grijs (PAG) en de rostrale ventromediale medulla (RVM) lopen projecties terug naar het ruggenmerg. Deze kunnen de volumeknop in lamina I, II en V omlaag draaien – of juist omhoog. Dit systeem kan pijn onderdrukken (endogene analgesie) of versterken (facilitatie).
Dit systeem wordt aangestuurd door:
- Prefrontale cortex (cognitieve controle: "Dit kunnen we aan")
- ACC (affectieve context: "Dit is niet gevaarlijk")
- Hypothalamus (stress, angst)
Dit is waarom soldaten soms geen pijn voelen bij ernstige verwondingen in een gevechtsituatie (massieve descenderende inhibitie, overleven heeft prioriteit), en waarom chronische pijnpatiënten juist overgevoelig kunnen zijn voor kleine prikkels (het systeem staat op faciliteren in plaats van afremmen ). Je brein heeft lettelijk een volume knop. Maar soms zet iemand hem op stand 11 en breekt de knop af.
Wanneer het systeem vastzit: chronische pijn
Bij acute pijn is dit systeem adaptief: het beschermt weefsel, stimuleert genezing, leert je gevaar te vermijden. Het past zich aan.
Maar bij chronische pijn treedt er plastische verandering op door het hele systeem (Kuner & Flor, 2016; Apkarian et al., 2011). En dan wordt het interessant. En ook vervelend.
👓Volg in de figuur de hele route van periferie naar cortex – bij chronische pijn gebeurt er reorganisatie op elk niveau:
Perifeer: nociceptoren worden overgevoelig (perifere sensitisatie)
Spinaal: in lamina I/V gaan de neuronen spontaan vuren, synapsen versterken, de inhibitie verzwakt (centrale sensitisatie)
Thalamisch: reorganisatie van somatotopische kaarten in VPL/VMpo
Corticaal: S1 ondergaat reorganisatie en toont structurele veranderingen, ACC wordt hyperactief, de prefrontale controle verzwakt, de anterieure insula toont veranderde activatipatronen.
Descenderende systemen: het PAG-RVM systeem (de groene pijlen) kan omslaan van inhibitie naar faciliteren – de rem verandert in een gaspedaal.
Het systeem evolueert van een alarm (alleen reactief) naar een producerend ‘machine': het brein produceert pijn, ook zonder weefselschade. Voorspel-fouten, prediction errors worden de norm. Het netwerk raakt gevangen in een staat waarin het verwacht pijn te voelen – en dus pijn blijft maken.
De hele anatomische route in de figuur blijft intact, maar de functie ervan verandert fundamenteel.
Het is alsof je een rookmelder hebt die besloten heeft dat alles brand is. Het brood dat je roostert? Brand. Een kaars aansteken? Brand. Iemand die een sigaret rookt drie straten verderop? Yep, ook brand.
Waarom dit verhaal belangrijk is
Dit causaal verhaal legt uit waarom:
1. Pijn geen directe maat is voor weefselschade – er zijn te veel verwerkingsstappen, te veel modulatie, te veel context. Pijn is geen barometer voor schade; het is een advies van je brein over hoeveel bescherming je nodig hebt
2. Chronische pijn niet "inbeelding" is – het is reële neuroplastische verandering in een echt systeem. Je brein heeft zich aangepast op een manier die niet meer adaptief is, maar het is even echt als die eerste keer dat je op dat legosteentje stapte.
3. Psychologische factoren niet “de softe sector" zijn – angst, verwachting, aandacht, betekenis moduleren op elk niveau, van ruggenmerg tot cortex. Dat is wetenschap, misschien anders te meten, wel een oorzaak -> gevolg.
4. Multimodale behandeling werkt – je kunt interveniëren op periferie (ontstekingsremming), ruggenmergniveau (epiduraal, neuromodulatie), descenderende paden (antidepressiva, beweging), en cognitief-emotioneel niveau (pijneducatie, exposure, ACT). Er zijn meerdere aangrijpingspunten in dit systeem.
Het brein maakt pijn – niet willekeurig, maar volgens regels. En als je die regels begrijpt, kun je leren ze te beïnvloeden.
Literatuur
Almeida, T.F., Roizenblatt, S., & Tufik, S. (2004). Afferent pain pathways: a neuroanatomical review. Brain Research, 1000(1-2), 40-56.
Apkarian, A.V., et al. (2005). Human brain mechanisms of pain perception and regulation in health and disease. European Journal of Pain, 9(4), 463-484.
Apkarian, A.V., et al. (2011). Chronic pain patients are impaired on an emotional decision-making task. Pain, 152(6), 1304-1314.
Baliki, M.N., & Apkarian, A.V. (2015). Nociception, pain, negative moods, and behavior selection. Neuron, 87(3), 474-491.
Basbaum, A.I., et al. (2009). Cellular and molecular mechanisms of pain. Cell, 139(2), 267-284.
Bushnell, M.C., et al. (2013). Cognitive and emotional control of pain and its disruption in chronic pain. Nature Reviews Neuroscience, 14(7), 502-511.
Craig, A.D. (2009). How do you feel--now? The anterior insula and human awareness. Nature Reviews Neuroscience, 10(1), 59-70.
Craig, A.D. (2015). How do you feel? An interoceptive moment with your neurobiological self. Princeton University Press.
Davis, K.D., et al. (2015). Brain imaging tests for chronic pain: medical, legal and ethical issues and recommendations. Nature Reviews Neurology, 11(4), 201-212.
Gauriau, C., & Bernard, J.F. (2002). Pain pathways and parabrachial circuits in the rat. *Experimental Physiology*, 87(2), 251-258.
Kuner, R., & Flor, H. (2016). Structural plasticity and reorganisation in chronic pain. *Nature Reviews Neuroscience*, 18(1), 20-30.
Legrain, V., et al. (2011). The pain matrix reloaded: a salience detection system for the body. *Progress in Neurobiology*, 93(1), 111-124.
Lorenz, J., et al. (2003). Keeping pain out of mind: the role of the dorsolateral prefrontal cortex in pain modulation. *Brain*, 126(5), 1079-1091.
Mancini, F., et al. (2012). Fine-grained nociceptive maps in primary somatosensory cortex. *Journal of Neuroscience*, 32(48), 17155-17162.
Ossipov, M.H., et al. (2010). Central modulation of pain. *Journal of Clinical Investigation*, 120(11), 3779-3787.
Peirs, C., & Seal, R.P. (2016). Neural circuits for pain: recent advances and current views. *Science*, 354(6312), 578-584.
Segerdahl, A.R., et al. (2015). The dorsal posterior insula subserves a fundamental role in human pain. *Nature Neuroscience*, 18(4), 499-500.
Shackman, A.J., et al. (2011). The integration of negative affect, pain and cognitive control in the cingulate cortex. Nature Reviews Neuroscience, 12(3), 154-167.
Todd, A.J. (2010). Neuronal circuitry for pain processing in the dorsal horn. Nature Reviews Neuroscience, 11(12), 823-836.
Torta, D.M., & Cauda, F. (2011). Different functions in the cingulate cortex, a meta-analytic connectivity modeling study. NeuroImage, 56(4), 2157-2172.
Vogt, B.A. (2016). Midcingulate cortex: structure, connections, homologies, functions and diseases. *Journal of Chemical Neuroanatomy, 74, 28-46.
Wiech, K. (2016). Deconstructing the sensation of pain: The influence of cognitive processes on pain perception. Science, 354(6312), 584-587.

